
Duplo sucesso no silenciamento do gene huntingtina por RNAi
2 boas notícias para o silenciamento genético por RNAi na DH: é seguro durante seis meses e existe uma forma de tratar áreas maiores do cérebro

Tem cuidado: Tradução automática – Possibilidade de erros
Para divulgar notícias sobre a investigação em DH e actualizações de ensaios ao maior número de pessoas possível e o mais rapidamente possível, este artigo foi traduzido automaticamente por IA e ainda não foi revisto por um editor humano. Embora nos esforcemos por fornecer informações exactas e acessíveis, as traduções da IA podem conter erros gramaticais, interpretações erradas ou frases pouco claras.Para obteres a informação mais fiável, consulta a versão original em inglês ou volta mais tarde para veres a tradução totalmente editada por humanos. Se detectares problemas significativos ou se fores um falante nativo desta língua e quiseres ajudar a melhorar as traduções exactas, não hesites em contactar-nos através de editors@hdbuzz.net
A maioria dos investigadores da DH está bastante entusiasmada com a ideia de ‘silenciar’ o gene da doença de Huntington, para reduzir a produção da proteína huntingtina nociva. Dois desafios – segurança e administração – estão agora mais perto de serem resolvidos graças ao trabalho colaborativo entre investigadores académicos e da indústria.
Somos grandes fãs do silenciamento genético. Como muitos investigadores da doença de Huntington, pensamos que é a abordagem com maior probabilidade de produzir um tratamento eficaz para a DH.
O silenciamento genético envolve a utilização de um medicamento especialmente concebido para intercetar uma molécula mensageira, chamada RNA, que é produzida a partir do gene DH e diz às células para produzirem a proteína huntingtina nociva. O efeito do medicamento é que as células produzem menos proteína.
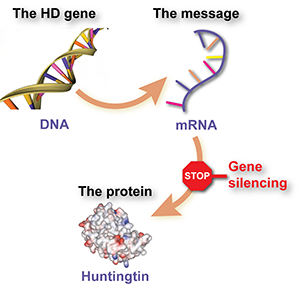
De forma ainda mais simples, o silenciamento genético é como um sinal de stop para a huntingtina mutante.
Progresso rápido
Até agora, o silenciamento genético para a DH, em várias formas, ultrapassou todos os obstáculos que encontrou. Já foi testado em vários modelos de DH em ratos e ratazanas, e não só abrandou a progressão como também produziu melhorias tanto nos sintomas como nos danos cerebrais. Parece que o cérebro pode realmente recuperar – até certo ponto – se os níveis da proteína nociva puderem ser reduzidos um pouco.
Os obstáculos restantes
Várias equipas de investigação estão a caminho de ensaios humanos de silenciamento genético na DH. Mas há alguns desafios restantes a resolver antes que isso possa acontecer.
O primeiro é a segurança. Efeitos secundários inesperados são sempre possíveis e podem ser dramáticos, já que estamos a falar de medicamentos que são injetados ou infundidos diretamente no sistema nervoso e interagem diretamente com a maquinaria genética das nossas células.
Outro é a administração. Os medicamentos de silenciamento genético não podem ser dados como comprimidos ou injeções no sangue, porque não seriam deixados entrar no cérebro. Por isso, têm de ser introduzidos diretamente no sistema nervoso. Dependendo da estrutura do medicamento, isto significa uma operação para introduzir agulhas ou tubos na coluna vertebral ou no crânio. Parece drástico, mas se o tratamento for eficaz, valerá a pena.
O problema da administração não acaba aí, porque uma vez que o medicamento está na cabeça, tem de entrar dentro das nossas células cerebrais para realizar a sua magia genética.
O menu do silenciamento genético
Os investigadores do silenciamento genético têm de fazer várias escolhas antes de iniciarem um ensaio de tratamento. Aqui está uma lista de verificação para te ajudar a compreender futuras notícias.
Primeiro, temos de decidir sobre a estrutura do medicamento. As duas escolhas básicas são medicamentos RNAi, que são quimicamente semelhantes às moléculas mensageiras RNA do corpo; e medicamentos ASO, que são ligeiramente diferentes mas podem ser melhor absorvidos pelas células.
A segunda escolha é qual o alvo a escolher: ambas as cópias do gene DH, ou apenas a mutante. Visar ambas – chamado silenciamento não específico – é mais fácil, mas desligar o gene ‘normal’ pode ser perigoso. Visar apenas o gene mutante – chamado silenciamento alelo-específico – pode ser mais seguro mas é muito mais difícil de fazer.
A terceira escolha é o destino – para onde irá o medicamento? Os medicamentos RNAi não se espalham naturalmente muito longe, por isso o medicamento tem de ser administrado diretamente na substância do cérebro. Medicamentos que se espalham mais, como os ASOs, podem ser infundidos no líquido à volta do cérebro ou, se tivermos sorte, na base da coluna vertebral.
Em quarto lugar, precisamos de decidir sobre a administração. O medicamento será dado sozinho, embalado num vírus ou bombeado sob pressão, para aumentar a sua dispersão pelo cérebro?
A quinta escolha é o regime de tratamento. Devemos dar um tratamento único ou infundir o medicamento durante semanas ou meses? Neste momento não sabemos quanto tempo durarão os efeitos, por isso isto tem de ser determinado comparando diferentes regimes.
Sempre que leres sobre investigação em silenciamento genético, é útil determinar logo à partida qual a opção que foi selecionada para cada uma destas escolhas.
Três chegam todos de uma vez
No recente Congresso Mundial de DH em Melbourne, o HDBuzz relatou apresentações empolgantes de vários grupos de investigação em silenciamento genético. Depois, em novembro, trouxemos-te notícias do primeiro ensaio de segurança do silenciamento do gene huntingtina usando RNAi num cérebro de primata.
“O medicamento RNAi espalhou-se mais do que conseguirias com simples injeções. Muito mais, na verdade.”
Agora, foram publicados dois artigos científicos adicionais – cada um fruto da colaboração entre investigadores académicos e empresas de biotecnologia. Ambos os artigos envolveram a empresa Medtronic, sediada em Minneapolis, e a equipa do Dr. Zheming Zhang da Universidade do Kentucky.
Segurança de seis meses
O relatório de novembro sobre a segurança do RNAi em primatas foi um estudo bastante curto – seis semanas. O novo estudo pela equipa da Medtronic e de Zhang, relatado na revista Brain, também foi feito em macacos rhesus, mas durou seis meses completos.
Vamos ver o que os investigadores estudaram, usando a lista de verificação acima:
-
Estrutura: este foi um ensaio de um medicamento RNAi.
-
Alvo: ambas as cópias do gene foram visadas – silenciamento não específico.
-
Destino: a substância do cérebro – o estriado, para ser exato, que é afetado precocemente nos doentes com DH.
-
Administração: o medicamento foi embalado num vírus vazio, chamado AAV2.
-
Regime de tratamento: uma injeção única em cinco locais em cada lado do cérebro
É também importante notar que foram usados macacos ‘normais’, sem cópias expandidas do gene DH. Por isso, este ensaio só podia medir alterações proteicas e segurança – não pode prever melhorias em doentes.
Após o tratamento, os macacos foram observados durante seis meses, observando a sua saúde geral e controlo do movimento. A cirurgia foi bem tolerada, e não foram observados novos problemas nos animais tratados.
Como esperado, os níveis de proteína huntingtina diminuíram significativamente nas regiões tratadas. Em cada local de injeção, os níveis de proteína foram reduzidos numa área de cerca de seis milímetros de diâmetro – em volume, isso é cerca do equivalente a três M&Ms por cérebro. Pode não parecer muito, mas num cérebro humano isso poderia fazer uma grande diferença, e lembra-te que estas medições foram feitas 6 meses após o tratamento único.
Felizmente, o medicamento não causou alterações cerebrais nocivas como inflamação, infeção ou danos neuronais.
Portanto, o medicamento fez o seu trabalho de reduzir os níveis de proteína, e o tratamento não pareceu produzir quaisquer efeitos nocivos. Os autores calculam que seis meses de macaco equivalem a cerca de 18 meses humanos. Parece bom – mas como os autores apontam, pode demorar ainda mais em humanos para que surjam efeitos bons ou maus.
Um método de administração inovador
O outro novo artigo veio de uma colaboração tripartida entre a equipa da Universidade do Kentucky, a Medtronic e a empresa de medicamentos RNAi Alnylam Pharmaceuticals. Foi publicado na revista Experimental Neurology.
Este foi também um estudo de silenciamento não específico por RNAi, administrado no estriado de macacos.
O que distingue este trabalho é o método de administração inovador. Foi usada uma técnica chamada distribuição aumentada por convecção (CED). Isto envolve colocar tubos através do crânio e na substância do cérebro. A extremidade superior do tubo está ligada a uma pequena bomba que constantemente injeta o medicamento pelo tubo sob pressão. Esta pressão é a chave – faz com que a molécula do medicamento se espalhe muito mais do que o faria de outra forma.

A CED já é usada para fazer com que medicamentos de quimioterapia se espalhem mais dentro de tumores cerebrais. Mas funcionaria para administrar um medicamento RNAi?
Primeiro, o medicamento foi bombeado para o cérebro durante sete dias. Apenas um lado do cérebro foi tratado, para que o outro pudesse ser usado para comparação. Foi usada uma gama de doses e taxas de infusão, para encontrar a melhor combinação. Depois, foi tentada uma infusão de 28 dias. De forma inteligente, a equipa fez modificações radioativas inofensivas ao medicamento, que lhes permitiram medir exatamente até onde se tinha espalhado.
O medicamento fez o seu trabalho de reduzir os níveis de huntingtina, e os tubos e infusões não prejudicaram particularmente o cérebro.
Mas será que o incómodo adicional de colocar tubos e bombas valeu a pena – será que o medicamento se espalhou mais? Em resumo, sim.
As medições mostraram que o medicamento RNAi alcançou muito mais longe do que seria de esperar com injeções simples. Se ambos os lados do cérebro tivessem sido tratados, os níveis de huntingtina teriam sido reduzidos no equivalente a cerca de onze M&Ms de cérebro.
Em resumo…
Antes destes dois artigos saírem, já sabíamos que a huntingtina podia ser reduzida no cérebro do macaco usando RNAi. Agora podemos adicionar dois grandes vistos à nossa lista de desejos: primeiro, o silenciamento funciona e é seguro durante períodos mais longos, e segundo, existem formas de fazer o medicamento espalhar-se mais.
O que poderia correr mal?
O otimismo cauteloso é uma abordagem sensata aqui. Há certamente algumas coisas que poderiam correr mal no caminho para os ensaios humanos, ou durante os mesmos.
Estes ensaios em primatas mostraram que reduzir os níveis de huntingtina é seguro em macacos saudáveis. Mas isso não significa que seja definitivamente seguro em doentes humanos. Os cérebros humanos são muito maiores e mais complexos do que os cérebros dos macacos. Por isso, o tratamento poderia ser menos eficaz, ou mais perigoso, simplesmente devido à diferença de espécie.
Também é possível que a proteína saudável proteja de alguma forma o cérebro do seu irmão nocivo em humanos. Se for esse o caso, silenciar ambas as cópias poderia inesperadamente fazer mais mal do que bem.
Os cérebros de pessoas com sintomas de DH são provavelmente mais frágeis e difíceis de operar, também. As partes do cérebro que precisam de tratamento são menores do que o normal, devido à atrofia causada pela DH. Por isso, as operações podem ser mais difíceis e mais arriscadas.
Finalmente, detetar o sucesso pode ser difícil em humanos, porque a doença progride lentamente, e não podemos examinar os cérebros dos doentes ao microscópio.
Mas nunca te esqueças – todos estes problemas estão a ser trabalhados em conjunto por algumas das melhores mentes científicas do mundo, todas focadas em tornar os tratamentos eficazes uma realidade para os doentes.
2012 – o ano do silenciamento genético para a DH?
Poderá 2012 ser o ano do silenciamento genético para os doentes com DH? Veremos um ou mais ensaios humanos nos próximos meses? Com base no progresso até agora, acreditamos realmente que isso é algo razoável para esperar, e vários grupos estão a trabalhar arduamente para torná-lo uma realidade. Os primeiros ensaios serão pequenos, e serão realizados lentamente e com grande cautela, porque a segurança é a principal preocupação. Mas se tudo correr bem, seguir-se-ão ensaios maiores.
Aprende mais
- Artigo na Brain sobre tratamento RNAi de 6 meses por Grondin e colegas (acesso livre)
- Artigo na Experimental Neurology sobre administração de RNAi por distribuição aumentada por convecção por Stiles e colegas (artigo completo requer pagamento ou subscrição)
- O nosso artigo sobre o ensaio anterior de segurança em primatas pela Dra. Beverly Davidson
Fontes e Referências
Para mais informações sobre a nossa política de divulgação, consulte as nossas FAQ…


