
Fazer bebés: ter uma família, à maneira da DH
Fazer bebés: artigo de destaque da HDBuzz – atualizado para 2024 – sobre tecnologias de fertilidade que podem ajudar pessoas em risco a terem filhos sem DH
Para pessoas em risco de doença de Huntington, ter um bebé que possa herdar a DH pode tornar as decisões sobre o planeamento familiar extremamente difíceis. Este artigo explica as opções disponíveis e como a ciência reprodutiva moderna pode fazer a diferença agora para as famílias afetadas pela DH.
Aviso de conteúdo Este artigo descreve questões de fertilidade, escolhas difíceis e procedimentos médicos, incluindo a interrupção da gravidez.
Nem todas as técnicas aqui descritas estão disponíveis em todos os lugares e, em alguns países, podem envolver grandes despesas. Portanto, se está a pensar em alguma delas, recomendamos que entre em contacto com um conselheiro genético especializado para obter aconselhamento individual. Quanto mais cedo o fizer, mais opções terá.

Introdução
Muitas pessoas com doença de Huntington, ou em risco de a contrair, gostariam de saber se existem maneiras de ter filhos sem transmitir a doença à próxima geração. A resposta curta é sim!
A ciência genética e as tecnologias reprodutivas significam que existem várias opções disponíveis para pessoas em risco de doença de Huntington, para garantir que os futuros filhos não corram o risco de desenvolver DH. Isto inclui pessoas que fizeram testes e são portadoras de uma expansão do gene da DH, mas também pode haver opções para algumas pessoas que optam por não fazer um teste genético para a DH.
Primeiro as coisas mais importantes: nada tem de mudar
Embora grande parte deste artigo se concentre nas opções para ter filhos sem DH, é importante saber que ter um filho sem fazer nenhum teste genético é uma opção para pais em risco de contrair a doença.
Como todos os artigos da HDBuzz confirmam, os cientistas estão a fazer progressos reais na procura de tratamentos para a doença de Huntington. Embora não possamos garantir nada ou prometer um cronograma firme, acreditamos firmemente que chegará um momento em que as crianças em risco nascerão num mundo onde a DH é uma doença tratável.
Além disso, há sempre uma hipótese de a criança não herdar a expansão do gene da DH em primeiro lugar e, portanto, nunca desenvolverá DH.
Algumas pessoas podem querer garantir filhos sem DH, mas as opções podem não estar disponíveis para elas, por exemplo, com base na localização, apoio financeiro ou crenças religiosas.
Ter um filho em risco de DH é algo que pode ser um ponto de discussão e debate dentro da comunidade da DH. Embora as pessoas possam não concordar com as decisões que os outros tomam, é importante lembrar que todos têm o direito de serem respeitados ao tomar as suas próprias decisões.
A Huntington Disease Youth Organisation tem alguns recursos disponíveis para ajudar a discutir a DH e o risco genético para as crianças de uma forma adequada à idade:
Algumas pessoas sentem que não querem correr riscos e gostariam de evitar o risco de transmitir a DH. É aí que entram as técnicas de testes genéticos. Estas opções estão disponíveis quer seja você ou o seu parceiro que está em risco de DH.
Quais são as minhas opções de testes genéticos?
Graças aos testes genéticos, podemos identificar o risco de DH para um feto durante uma gravidez ou em embriões no laboratório.
Testar um feto durante a gravidez é chamado de teste pré-natal. Testar embriões no laboratório é uma forma de fertilização in vitro ou FIV, e é chamado de teste genético pré-implantação ou PGT.
Se você ou o seu parceiro fizeram um teste genético que confirma que são portadores de uma expansão do gene da DH, poderá fazer um teste direto durante a gravidez ou através de PGT, para confirmar se a gravidez ou o embrião herdaram ou não a expansão do gene da DH.
Algumas pessoas querem filhos sem DH sem fazer o teste genético. Existem opções para isso também! Elas envolvem versões mais complicadas dos mesmos métodos. Então, primeiro vamos discutir como funciona para casais onde um dos parceiros já fez um teste genético positivo para DH.
Teste Genético Pré-implantação (PGT)
O teste genético pré-implantação é uma forma de ter um filho sem DH sem ter de considerar a interrupção de uma gravidez. No entanto, pode ser um processo longo, desafiador e caro.
O PGT envolve o uso de óvulos e espermatozoides para criar embriões num laboratório, depois realizar o teste de DH nos embriões e colocar apenas os embriões negativos para DH no útero.
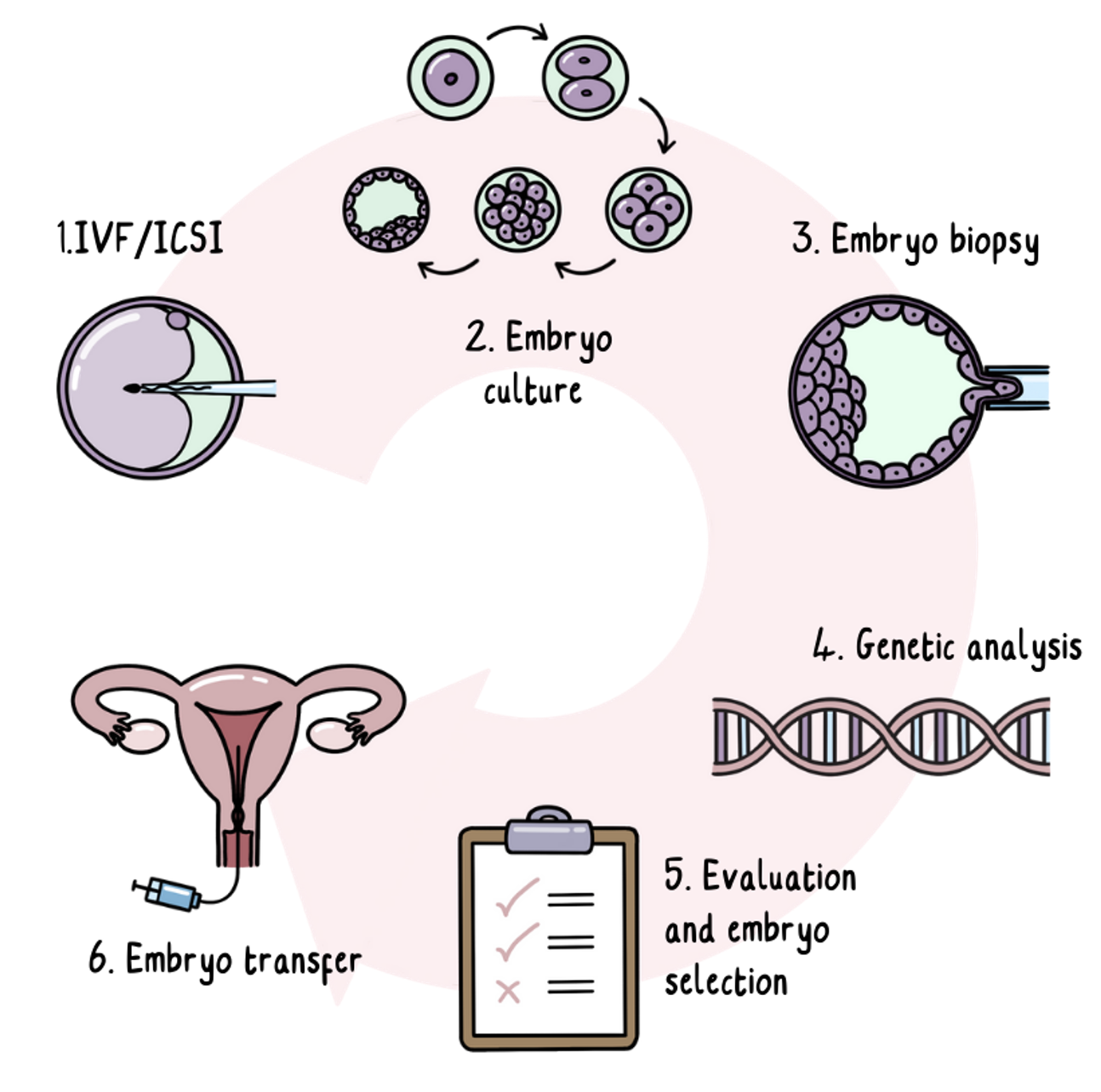
O Processo de PGT
O PGT é a FIV com uma etapa adicional de testes genéticos. A FIV é um procedimento médico que envolve uma medicação hormonal para fazer com que o fornecedor de óvulos produza mais óvulos do que o normal. A medicação hormonal pode envolver injeções para administrar os medicamentos no corpo.
Os óvulos são então recolhidos e fertilizados usando uma amostra de esperma.
Os óvulos fertilizados desenvolvem-se em embriões, que são cultivados no laboratório por até cinco dias até serem um pequeno conjunto de células. Uma ou duas células são removidas de cada embrião nesta fase e enviadas para testes genéticos enquanto os embriões são congelados e armazenados. Remover células nesta fase inicial de desenvolvimento não afeta a forma como o embrião se desenvolve.
Quaisquer embriões que não corram o risco de desenvolver DH continuarão a ser armazenados. Dependendo do país em que se encontra, um ou dois destes embriões sem risco são então transferidos para o útero.
Cerca de duas semanas após a transferência dos embriões, é realizado um teste de gravidez numa amostra de sangue. Se a transferência tiver sido bem-sucedida, a gravidez continua normalmente.
O lado negativo do PGT
O processo de estimular a libertação de óvulos, recolher óvulos, fertilizá-los fora do corpo e devolver embriões ao útero – é sempre um processo demorado e exaustivo. Também pode ser perigoso, acarretando riscos de a pessoa ficar doente.
Várias coisas podem correr mal, como não serem produzidos óvulos ou embriões suficientes. Também há mais hipóteses de ter gémeos com PGT, o que é mais difícil e arriscado.
Além dos riscos do procedimento, as coisas podem correr mal com a parte genética do PGT. Os embriões podem ser danificados quando as células são removidas e, por vezes, o teste de DH não funciona porque não há ADN suficiente. A má sorte pode significar que todos os embriões têm a mutação da DH.
Crédito da imagem: @gcnotes
No final, por vezes, apenas um embrião está disponível para implantação – e, por vezes, nenhum. Para piorar a situação, uma gravidez pode falhar após a implantação. No geral, cada tentativa de PGT dá uma probabilidade de 20-30% de uma gravidez sem DH. Esta taxa de sucesso varia por centro de PGT e depende de vários fatores.
As mulheres com menos de 35 anos têm as taxas de sucesso mais elevadas – outra razão para pensar no futuro sobre a fertilidade. Infelizmente, as hipóteses de sucesso acima dos 40 anos são pequenas.
Quanto custa o PGT?
O PGT é caro. O custo é algures na região de 20.000 dólares americanos (15.000 libras esterlinas ou 18.000 euros) por cada tentativa.
O seguro de saúde geralmente não cobre o custo do PGT/PGD. Em alguns países, o sistema público de saúde financia algumas tentativas de PGT – por exemplo, três tentativas no Reino Unido – mas mesmo isto pode variar dentro de cada país e pode ser limitado a casais sem filhos existentes.
Quaisquer embriões adicionais que não corram o risco de DH podem ser armazenados. No entanto, isto também tem um custo que varia dependendo do tempo de armazenamento.
Se esta é uma opção que está a considerar, recomendamos que entre em contacto com o seu serviço genético local para ter uma discussão sobre elegibilidade, encaminhamento e custos associados.
Testes durante a Gravidez
É possível realizar um teste genético durante a gravidez para ver se o bebé em desenvolvimento (feto) é portador da expansão do gene que causa a DH. Isto chama-se teste pré-natal.
Decidir se deve testar um feto é uma decisão difícil. É importante entender que o teste pré-natal na DH só é realizado sob o entendimento de que, se o resultado mostrar que o feto é portador da expansão do gene da DH, a gravidez será interrompida. Esta é uma escolha imensamente desafiadora e pessoal.
É importante pensar cuidadosamente sobre o teste pré-natal para DH e como se sente em relação à interrupção da gravidez, antes de engravidar.
Uma vez grávida, há muito pouco tempo para absorver as informações sobre o teste pré-natal e tomar estas decisões importantes, pois o teste tem de ser realizado no início da gravidez.
Testar uma gravidez, mas não prosseguir com uma interrupção após um resultado positivo no teste, retiraria o direito da criança de escolher se quer fazer o teste genético, mais tarde na vida. Afinal, a maioria das pessoas em risco de DH opta por não fazer o teste antes de desenvolver sintomas. Sabemos que podem ocorrer grandes problemas quando uma criança é identificada, desde o nascimento, como alguém que irá desenvolver DH.
Além disso, a maioria dos testes na gravidez só pode ser feita se os testes tiverem sido realizados no casal ou noutros membros da família antes. Muitas vezes, não há tempo suficiente para fazer este trabalho de fundo quando uma gravidez já começou.
Teste Pré-natal Invasivo
Mais comum e fiável, um procedimento chamado amostragem de vilosidades coriónicas ou CVS é realizado durante o início da gravidez para testar o feto. O CVS envolve a recolha de uma pequena amostra da placenta que representa o ADN no feto.
O CVS é um procedimento rápido na clínica ambulatorial e, em alguns países, é feito sob anestesia local. Dependendo de onde a placenta está presa à parede do útero, uma agulha muito fina é passada através do colo do útero ou através da pele do abdómen, usando um scanner de ultrassom para guiá-la. Uma pequena amostra de células é então recolhida da placenta.
Estas células podem ser usadas para testar a expansão do gene da DH. Alguns centros genéticos também oferecem testes para três síndromes cromossómicas comuns como parte do teste genético CVS.
O CVS é geralmente realizado entre 11 e 12 semanas de gravidez, mas não mais tarde do que 15 semanas. Uma ecografia precoce é frequentemente necessária antes de um CVS ser realizado.
A principal complicação deste procedimento é um pequeno risco de aborto espontâneo. Cada centro terá informações específicas sobre o risco de aborto espontâneo após um CVS. Entre em contacto com o seu centro local se desejar saber mais.
Uma amniocentese é outro tipo de técnica de teste pré-natal invasivo, semelhante a um CVS, mas retira uma amostra de líquido amniótico em vez de placenta. Isto pode ser realizado a partir das 16 semanas. Isto, portanto, fornece um resultado numa gestação muito posterior e pode tornar as decisões sobre a interrupção da gravidez ainda mais desafiadoras.
Se o teste genético for positivo, uma interrupção pode geralmente ser realizada sob anestesia geral até cerca de 12-13 semanas, dependendo das leis do país. Infelizmente, por vezes, pode haver uma lista de espera para este procedimento.
Em alguns países, a interrupção da gravidez pode ser realizada mais tarde, induzindo o parto; no entanto, a disponibilidade desta opção depende novamente das leis do país.
E se eu não quiser fazer o teste genético?
Existem maneiras de ter filhos sem DH sem que o parceiro em risco seja testado.
Eles usam os mesmos métodos básicos que descrevemos – teste pré-natal ou PGT – com uma reviravolta genética para identificar gravidezes ou embriões de ‘alto risco’ sem revelar o estado do gene da DH do parceiro em risco.
A reviravolta é um par de métodos chamados teste de exclusão ou teste de não divulgação. Estes envolvem mais preparação e planeamento, e há algumas situações em que não é possível, então, se isto lhe parece a opção certa: obtenha aconselhamento especializado cedo.
Como funciona o teste de exclusão?
O teste de exclusão envolve pelo menos três amostras de sangue. Uma de cada do casal que deseja aumentar a sua família e, idealmente, uma de cada da mãe e do pai da pessoa em risco de desenvolver DH. Esta técnica pode, por vezes, não ser uma opção sem uma amostra de sangue do progenitor afetado com DH.
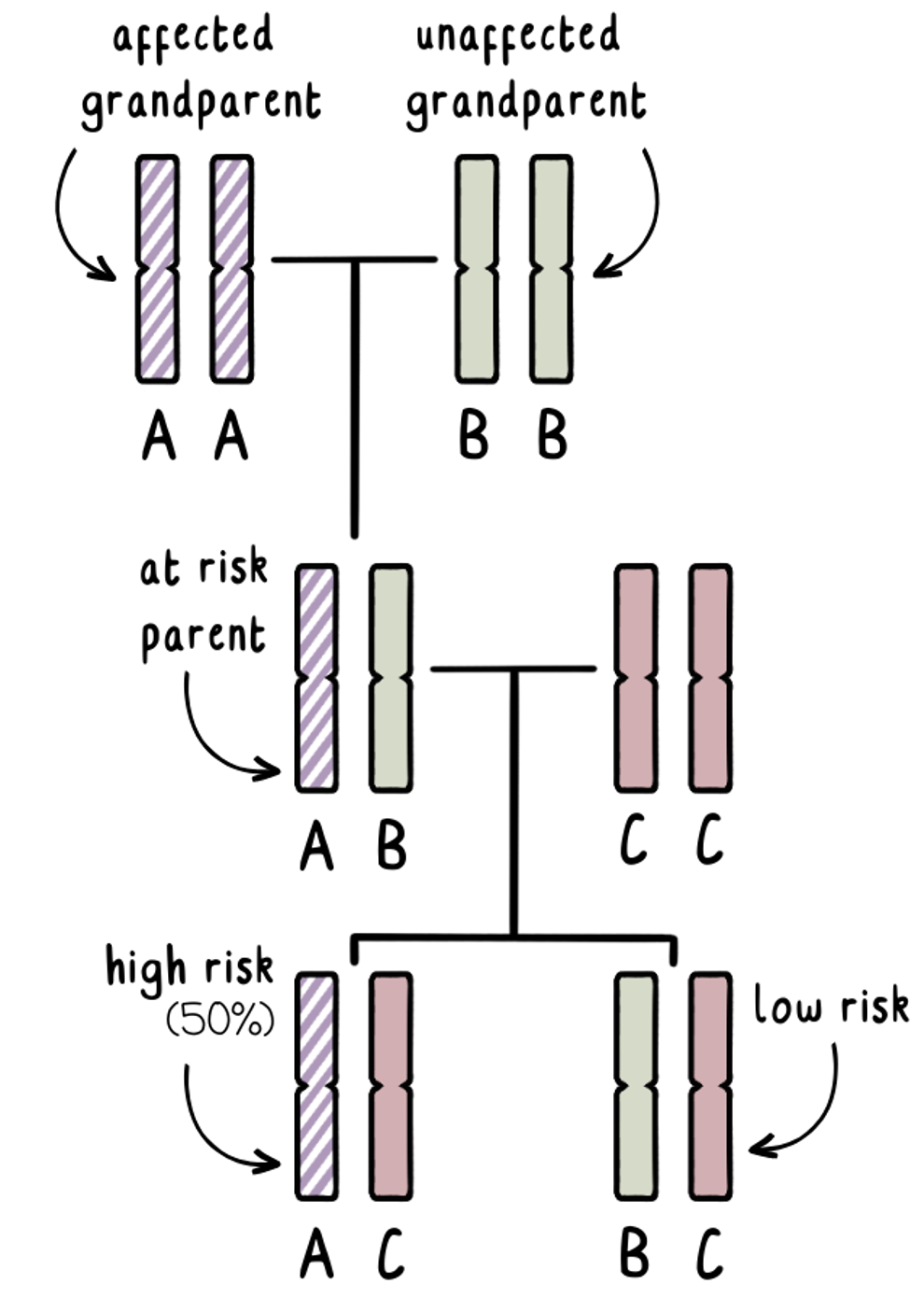
Sabemos que cada um de nós herdará uma cópia do gene da DH de cada progenitor. O avô afetado terá uma cópia normal do gene da DH e uma cópia expandida do gene da DH. Podemos rotular estes genes como ‘AA’. Não sabemos qual deles foi transmitido ao seu filho adulto – e essa pessoa não quer ser testada para descobrir.
Crédito da imagem: @gcnotes
O avô não afetado terá duas cópias normais do gene da DH. Podemos chamá-los de ‘BB’.
O adulto em risco terá alguma combinação de A e B, com o gene A tendo uma probabilidade de 50% de transportar a mutação.
Se eles desejam ter uma família sem fazer testes genéticos para determinar o seu próprio risco, podemos usar o teste de exclusão durante um teste pré-natal ou PGT para identificar se o feto ou embrião herdou um gene A do avô afetado, ou um gene B do avô não afetado. Isto diz-nos se a gravidez seria de alto risco ou de baixo risco.
Crucialmente, o teste de exclusão identifica o avô de origem, sem nos dizer se o gene da DH expandido foi herdado. Se descobrimos a resposta para isso, poderia dizer-nos os resultados do progenitor em risco – que é o que estamos a tentar evitar!
O outro lado disto é que alguns embriões de alto risco não transportam uma mutação da DH, o que significaria potencialmente terminar uma gravidez ou descartar embriões que podem não ter estado em risco de DH em primeiro lugar.
PGT de não divulgação
A não divulgação é uma reviravolta no PGT que permite que pessoas em risco tenham filhos sem DH sem descobrir o seu próprio estado genético. Esta opção não está disponível em todos os países, por isso é importante entrar em contacto com o seu serviço genético local para saber se esta é uma opção disponível na sua área.
Se um casal em risco optar pelo PGT de não divulgação, a amostra de sangue da pessoa em risco seria testada para a mutação da DH. A pessoa em risco não seria informada do resultado deste teste, nem nenhum dos profissionais de saúde que a pessoa em risco encontra – apenas os profissionais do laboratório de fertilidade saberiam o resultado.
O PGT começa então, com a recolha de óvulos e a geração de embriões. Se o resultado do teste ‘secreto’ da pessoa em risco mostrar que ela tem uma expansão do gene da DH, os embriões são testados para DH e apenas aqueles sem a expansão do gene da DH são transferidos para uma potencial gravidez.
O casal não é informado sobre quantos óvulos são recolhidos, quantos são fertilizados com sucesso ou quantos embriões são implantados. Se não houver embriões sem uma expansão do gene da DH, o ciclo termina aí, e o casal é informado de que a fertilização falhou, mas não é dito o motivo.
A FIV pode falhar por muitas razões, por isso uma falha na gravidez não pode ser interpretada como significando que a pessoa em risco tem o gene da DH.
Outras opções
Uma forma de ter filhos sem DH é usar óvulos ou esperma de dadores em vez dos da pessoa em risco. Decidir ter um filho com a ajuda de um dador é uma decisão difícil, mas evita a necessidade de considerar a interrupção de uma gravidez. Pode ser feito para pessoas que fizeram um teste preditivo mostrando que têm uma expansão do gene da DH, bem como para aquelas em risco que não querem ser testadas.
Como todas as escolhas, esta é complicada. A criança não estará geneticamente relacionada com o progenitor em risco, e será necessário pensar cuidadosamente sobre como e quando partilhar a informação com a criança. Um progenitor não precisa de estar geneticamente relacionado com o seu filho para cumprir um papel parental completo e amoroso. Há muito apoio disponível para as pessoas que decidem seguir esta via, e isto pode ser discutido antes de decidir embarcar no processo.
Muitos casais pensam em adotar crianças. Em muitos lugares, os casais em que um dos parceiros está em risco de DH podem ter dificuldade em adotar uma criança. Isto deve-se à doença estar na família e a agência de adoção ter de garantir que a criança tem um lar estável para onde ir. No entanto, cada caso é avaliado individualmente, por isso vale a pena considerar a adoção como uma opção. Se tiveres sido recusado para adoção, os casais em risco podem ser capazes de ser pais de acolhimento para crianças, já que esta é frequentemente uma opção de curto prazo, cuidando de crianças durante semanas ou meses de cada vez. O tempo que passas com crianças de acolhimento, embora curto, pode ainda ter um impacto positivo na vida da criança.
Direções Futuras
O Diagnóstico Pré-Natal Não Invasivo é uma forma mais recente de testar durante a gravidez sem fazer um teste invasivo, evitando assim o pequeno risco de aborto espontâneo. Em vez de um teste invasivo que recolhe uma amostra da placenta ou do líquido amniótico, o DPNI recolhe uma amostra de sangue do progenitor que está grávido. Este teste procura pequenos fragmentos de ADN do feto que circulam no sangue dos progenitores.
O DPNI pode ser realizado a partir das 10 semanas de gravidez. O DPNI geralmente envolve algum trabalho preparatório pelo laboratório antes de uma gravidez. Requer amostras do casal que pretende aumentar a família e pode requerer uma amostra de um familiar afetado.
O DPNI já está disponível na clínica para algumas doenças hereditárias e está em desenvolvimento para a DH, mas atualmente não está amplamente disponível. Há vários casos em que o DPNI não seria apropriado, por exemplo, durante gravidezes gemelares. Se e quando o DPNI para a DH estiver disponível, é provável que um resultado indicando que uma gravidez está em risco de DH ainda seja seguido por um teste invasivo para confirmar os resultados do teste, antes de marcar uma interrupção.
E quanto às pessoas LGBTQIA+?
Todas as opções discutidas acima são provavelmente disponíveis para casais LGBTQIA+, com um histórico familiar de DH, que estão a procurar começar uma família. Haveria o passo adicional de encontrar um dador de esperma ou óvulos, bem como uma barriga de aluguer, se necessário, o que virá com o seu próprio custo adicional e documentação legal.
Em muitos países, ser LGBTQIA+ é pouco provável que te impeça de aceder à opção de planeamento familiar que é certa para ti e para o teu parceiro. Haverá informações específicas sobre as técnicas de planeamento familiar disponíveis no teu país para casais LGBTQIA+ que desejam ter uma família.
Resumo
Há várias opções disponíveis para pessoas em risco de DH que desejam começar uma família.
Nem todos escolhem passar por testes genéticos para começar uma família, e esta é uma opção completamente válida.
Para aqueles que desejam remover o risco de o seu filho herdar a DH, podem não precisar de saber o seu próprio risco de DH. O teste direto pode ser realizado quando sabemos o resultado do progenitor em risco e é demonstrado que têm a expansão do gene da DH. Por outro lado, o teste de exclusão ou não divulgação pode ser realizado para casais em risco que não desejam descobrir os seus próprios resultados de teste.
Os testes diretos e de não divulgação podem ser realizados durante o teste genético pré-implantação (PGT), onde os embriões são criados em laboratório e testados quanto ao seu risco de desenvolver DH, ou um feto pode ser testado durante a gravidez. O teste na gravidez pode ser invasivo através da amostra de vilosidades coriónicas (CVS) ou não invasivo (DPNI), mas ambas estas opções são apenas para aqueles que considerariam terminar uma gravidez em risco de desenvolver DH.
Existem outras opções disponíveis para casais em risco que incluem o uso de óvulos/esperma de dadores ou a adoção/acolhimento de crianças.
O aconselhamento especializado, na forma de aconselhamento genético, ajudar-te-á a compreender as opções exatas disponíveis localmente e a explorar qual a opção que te parece mais adequada. A Associação de DH do teu país pode dizer-te como entrar em contacto com um conselheiro genético. Como em tantas coisas na vida, o planeamento antecipado e a compreensão de todas as opções com antecedência é fundamental.
Aprende mais
- Página da Genetic Alliance (Reino Unido) sobre testes genéticos pré-implantação
- National Society of Genetic Counselors (EUA). Encontre um conselheiro genético online. O teu médico de família ou a Associação regional de DH também podem aconselhar-te sobre como ser encaminhado para um conselheiro genético para discutir opções de fertilidade.
- O guia da Human Fertility and Embryology Authority sobre fertilidade assistida para pessoas que vivem com condições genéticas (Reino Unido)
Fontes e Referências
Para mais informações sobre a nossa política de divulgação, consulte as nossas FAQ…


