
Atualização confirma que o ensaio de ‘silenciamento genético’ da doença de Huntington está no caminho certo
A Ionis afirma que o seu ensaio do HTTRx, destinado a reduzir a proteína huntingtina, está totalmente recrutado e planeia prolongá-lo

A Ionis Pharmaceuticals lançou o primeiro ensaio de um medicamento para reduzir a huntingtina – por vezes chamado de ‘medicamento de silenciamento genético’ – no final de 2015. Numa atualização significativa, a empresa anunciou dois marcos importantes: o ensaio está agora totalmente recrutado, e uma ‘extensão de rótulo aberto’ será ativada para os voluntários no ensaio atual. Embora nada seja garantido, isso é um bom presságio para o futuro deste importante programa.
Um rápido resumo sobre a redução de huntingtina
A ideia de ‘desligar’ a causa da doença de Huntington foi um dos primeiros pensamentos que surgiram na cabeça dos investigadores quando o gene HD foi descoberto em 1993.
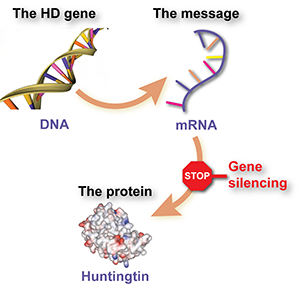
O primeiro grande progresso na obtenção disso ocorreu há cerca de uma década, quando vários estudos em ratos relataram sucesso na redução da atividade do gene. Ao fazer isso, os níveis da proteína para a qual o gene é uma receita foram reduzidos:
Esses medicamentos para reduzir a huntingtina atuam de maneiras semelhantes – ao ‘eliminar o mensageiro’. Um gene é uma receita para uma proteína, mas entre o gene e a proteína, é feito um mensageiro químico que é essencialmente uma cópia funcional do gene. Eliminar o mensageiro interrompe a linha de produção, de modo que menos proteína é produzida.
Os medicamentos para reduzir a huntingtina são feitos de moléculas semelhantes ao ADN, o material que compõe os nossos genes. Este tipo de substância química tem a capacidade especial de se ligar fortemente entre si, se a sequência de ‘letras’ genéticas coincidir corretamente. Os fabricantes de medicamentos podem construir moléculas personalizadas com uma sequência que se ligará à molécula mensageira do gene huntingtina, mas não a outros mensageiros.
Quando a célula percebe que o mensageiro tem uma molécula de medicamento ligada a ele, reconhece que algo incomum aconteceu e responde eliminando a molécula mensageira. Eventualmente, isso reduz o nível da proteína.
As próprias moléculas do medicamento vêm em muitos tipos diferentes. Algumas são feitas de ARN (o material de que o mensageiro é feito), enquanto outras são feitas de ADN (o material de que os nossos genes são feitos).
Uma palavra rápida sobre terminologia. Muitas pessoas, incluindo o HDBuzz, referiram-se a estes como medicamentos de ‘silenciamento genético’. Isso sugere ligeiramente que estamos a tentar desligar o gene por completo, o que provavelmente não é possível ou desejável. Assim, cada vez mais, ouvirão-nos chamá-los de medicamentos de ‘redução de huntingtina’. Ainda usaremos a expressão ‘silenciamento genético’ de vez em quando, para que as pessoas possam encontrar o artigo mais recente se pesquisarem o termo mais conhecido.
O ensaio atual
Quando começaram a trabalhar no HD há mais de uma década, a empresa californiana por trás do ensaio atual chamava-se Isis Pharmaceuticals. Muita coisa mudou desde então, incluindo o nome da empresa – desde 2015 chama-se Ionis.
O medicamento da Ionis é um oligonucleotídeo antisense, ou ASO. Isso significa que é uma única cadeia de ADN quimicamente modificado, projetada para se ligar à molécula mensageira do gene huntingtina.
Só para manter as coisas emocionantes, o próprio medicamento tem dois nomes. Inicialmente foi chamado de ISIS-443139, mas ultimamente tem sido chamado de IONIS-HTTRx ou apenas HTTRx – uma combinação de HTT, a abreviatura que os cientistas usam para o gene huntingtina, e Rx, um símbolo usado na indústria farmacêutica que significa tratamento ou prescrição.
“O estudo de extensão de rótulo aberto estará disponível apenas para voluntários no ensaio atual.”
(Curiosidade: a origem de ‘Rx’ é desconhecida, mas pode vir da palavra latina ‘receita’.)
O ensaio da Ionis, liderado em parceria com a Prof. Sarah Tabrizi da University College London, foi a primeira vez que um medicamento direcionado para reduzir a huntingtina foi testado em humanos. Como no primeiro ensaio de qualquer novo medicamento, o principal foco do ensaio é a segurança.
Para chegar ao cérebro, medicamentos ASO como o HTTRx têm de ser injetados no fluido espinhal usando uma agulha fina. Isso é chamado de injeção intratecal. Embora isso possa parecer horrível, é um método comumente usado para tratar o cérebro em outras condições, como o cancro. Um procedimento intimamente relacionado – punção lombar ou punção espinhal – é muito amplamente utilizado, e de facto, muitas centenas de voluntários de famílias com doença de Huntington já passaram por este procedimento para doar fluido espinhal valioso para ajudar na investigação do HD.
O ensaio de segurança atual do HTTRx envolve pacientes com sintomas iniciais da doença de Huntington. Após uma avaliação clínica extensa, cada voluntário recebe quatro injeções do medicamento em intervalos mensais, seguidas por uma coleta final de fluido espinhal.
Ao longo do ensaio, foi utilizado um braço de placebo, para ajudar a distinguir os efeitos do medicamento dos efeitos de estar no ensaio, como o procedimento de injeção. O ensaio tem um design de escalonamento de dose: doses muito baixas foram administradas inicialmente, com voluntários posteriores recebendo doses mais altas.
O que há de novo
O comunicado de imprensa de hoje da Ionis – a primeira atualização oficial desde o início do ensaio – traz notícias cautelosamente otimistas. Contém dois anúncios importantes. Primeiro, o recrutamento para o ensaio atual está completo. E segundo, a empresa está a lançar uma extensão de rótulo aberto para o ensaio atual.
A conclusão do recrutamento é um marco importante para qualquer ensaio, mas para este é particularmente significativo. O ensaio envolveu uma série de ‘primeiros’ – o primeiro medicamento ASO administrado a pacientes com HD, a primeira vez que a injeção intratecal foi usada no HD – e cada escalonamento de dose trouxe tanto a esperança de benefícios mais fortes quanto um maior risco de efeitos indesejados.
Ao longo de um ensaio como este, um comité independente de especialistas analisa regularmente todos os dados de segurança para procurar qualquer sinal de perigo ou dano. A notícia de que o ensaio está totalmente recrutado e os últimos pacientes estão a passar pelos procedimentos é uma forte sugestão de que, mesmo nas doses mais altas, a segurança do medicamento parece boa. Apesar dos testes de segurança exaustivos antes de entrar em pacientes, qualquer medicamento pode produzir efeitos indesejados, por isso essa é realmente a melhor notícia que poderíamos esperar ouvir nesta fase.
Nas palavras do comunicado de imprensa: “O perfil de segurança e tolerabilidade do IONIS-HTTRx nos grupos concluídos do estudo de Fase 1/2a apoia o seu desenvolvimento contínuo”. Polegares para cima para isso da nossa parte.

Com o recrutamento completo, a Ionis está agora em posição de definir um cronograma para a conclusão do ensaio e o primeiro lançamento dos seus resultados. “Resultados principais” são esperados por volta do final de 2017. Na nossa experiência, os resultados de um ensaio como este podem não sair todos de uma vez. Os dados de segurança podem vir primeiro, mas informações sobre se o tratamento com HTTRx reduziu o nível da proteína huntingtina no fluido espinhal – um resultado ‘biomarcador’ muito aguardado – podem demorar um pouco mais a materializar-se.
Uma extensão de rótulo aberto
O ensaio atual do HTTRx tem um design cego: alguns voluntários receberam quatro injeções sem medicamento ativo – e nem os pacientes nem o pessoal do ensaio sabiam quem estava a receber medicamento ou placebo.
Num ensaio de extensão de rótulo aberto, ou OLE, os voluntários de um ensaio cego são convidados a voltar para mais doses, e cada voluntário recebe o medicamento ativo em vez de alguns receberem medicamento e outros placebo – geralmente na dose mais alta que foi testada com segurança no ensaio cego.
A Ionis já tinha dito que uma extensão de rótulo aberto poderia ser implementada se os dados do ensaio de segurança fossem bons. Não queremos ler muito num anúncio breve, mas realizar um OLE não é barato para um patrocinador de ensaio, por isso este anúncio certamente nos dá otimismo sobre todo o programa HTTRx.
O estudo de extensão de rótulo aberto estará disponível apenas para voluntários no ensaio atual. Isso significa que será realizado nos mesmos centros de estudo no Reino Unido, Canadá e Alemanha. A duração e o design exato do OLE ainda não foram anunciados, mas fornecerá uma riqueza de informações que a Ionis e o seu parceiro, Roche, podem usar para planear os seus próximos passos.
Agradecendo aos nossos heróis
Um benefício importante de uma extensão de rótulo aberto é que recompensa os voluntários que participaram no estudo original, dando-lhes acesso garantido ao medicamento ativo. Estamos particularmente satisfeitos com este aspeto do anúncio. Os participantes neste ensaio eram todos membros de famílias com doença de Huntington que dedicaram tempo significativo para receber injeções espinhais de um medicamento que, no início do ensaio, nunca tinha sido administrado a humanos antes. Aqueles que se inscreveram mais tarde receberam doses mais altas do que qualquer outra pessoa tinha recebido anteriormente.
Independentemente do resultado, esses voluntários aceitaram riscos pessoais, e na maioria dos casos fizeram-no para ajudar os outros em vez de si mesmos. Toda a nossa comunidade deve a esses heróis uma dívida de gratidão pela sua coragem e serviço. Por favor, junte-se a nós para saudá-los nas redes sociais usando a hashtag #HDResearchHeroes.
O que vem a seguir?
A Ionis disse: “o próximo passo para este programa será realizar um estudo para investigar se a diminuição da proteína huntingtina mutante com o IONIS-HTTRx pode retardar a progressão desta terrível doença.”
A extensão de rótulo aberto começará em breve, provavelmente nos próximos meses. Os voluntários no ensaio de segurança serão contactados pelos locais de estudo, com informações sobre como e quando podem inscrever-se para o OLE. Entretanto, aqueles participantes que ainda estão no ensaio cego precisarão de terminar a sua participação antes de passarem para a extensão de rótulo aberto.
Se não participou no ensaio de segurança cego, não poderá inscrever-se para a extensão de rótulo aberto. Por favor, não contacte os locais de estudo, a menos que tenha participado no ensaio original.
No final de 2017, podemos esperar ouvir um anúncio oficial sobre os resultados do ensaio cego. Não fique desapontado se isso se limitar a dados de segurança na primeira instância. “Seguro e bem tolerado” deve ser música para os ouvidos dos membros da família HD após um ensaio deste tipo!
Mais tarde, talvez no início de 2018, pode haver um anúncio separado sobre alguns dos resultados mais experimentais do ensaio de segurança – coisas como se o HTTRx reduziu o nível de huntingtina no fluido espinhal.
A próxima grande notícia, se tudo continuar a correr bem, pode ser o anúncio de um ensaio de eficácia, testando o HTTRx por tempo suficiente para determinar se retarda a progressão da doença. A Roche agora tem o direito de optar por participar, assumir o desenvolvimento do medicamento e realizar tal ensaio com base no seu próprio processo de tomada de decisão. Com um pouco de sorte, podemos ouvir sobre isso nos próximos meses também.
Enfatizando o seu desejo de avançar com o medicamento, em um anúncio separado feito diretamente à comunidade HD, a Ionis disse “Após a conclusão do estudo, o próximo passo para este programa será realizar um estudo para investigar se a diminuição da proteína huntingtina mutante com o IONIS-HTTRx pode retardar a progressão desta terrível doença.”
Até agora, não temos ideia de quando o próximo grande estudo começará, mas o nosso melhor palpite seria no final de 2018 ou início de 2019. Quanto ao quando, quantos pacientes, e em que países e locais – é muito cedo para ter certeza, mas a Ionis diz “Os estudos futuros para o programa serão realizados globalmente e incluirão locais de estudo nos EUA“. Quanto ao resto, pode ter certeza de que lerá sobre isso primeiro no HDBuzz.
Nada acontece rápido o suficiente para as pessoas cujas famílias são afetadas pelo HD – mas este é um momento para pausar e ficar feliz que, para este importante programa de redução de huntingtina, as notícias até agora são todas boas.
Aprende mais
Para mais informações sobre a nossa política de divulgação, consulte as nossas FAQ…


