Pequenos cérebros cultivados em laboratório revelam informações sobre a doença de Huntington e como a podemos tratar
Novas descobertas empolgantes usando mini cérebros humanos cultivados em 3D em laboratório informam os ensaios em curso de redução de HTT e sugerem que os transplantes de células estaminais para a DH podem melhorar a comunicação célula a célula e reduzir as características da doença.

As células estaminais cultivadas em 3D num laboratório de investigação podem imitar algumas características da doença de Huntington (DH). Também são promissoras para estudos de transplante para potencialmente repor células que são perdidas na DH. Mas o que aconteceria a essas novas células? Dar-se-iam bem com as células ainda presentes no cérebro que têm o gene da DH? E o que pode este sistema ensinar-nos sobre os ensaios clínicos em curso que visam reduzir a mensagem causadora da DH apenas em partes do cérebro? Continua a ler para descobrir!
O poder das células estaminais
As células estaminais têm um certo misticismo. Podem manter o seu estado “estaminal”, permanecendo uma célula estaminal, ou transformar-se em algo completamente diferente. Cada uma contém a capacidade de se tornar em quase qualquer tipo de célula do corpo humano. Os cientistas podem induzi-las a tornarem-se numa célula cardíaca, ou numa célula muscular, ou até numa célula cerebral, fornecendo aos cientistas uma poderosa ferramenta de investigação que pode ser usada para responder a questões sobre os cérebros das pessoas na saúde e na doença.
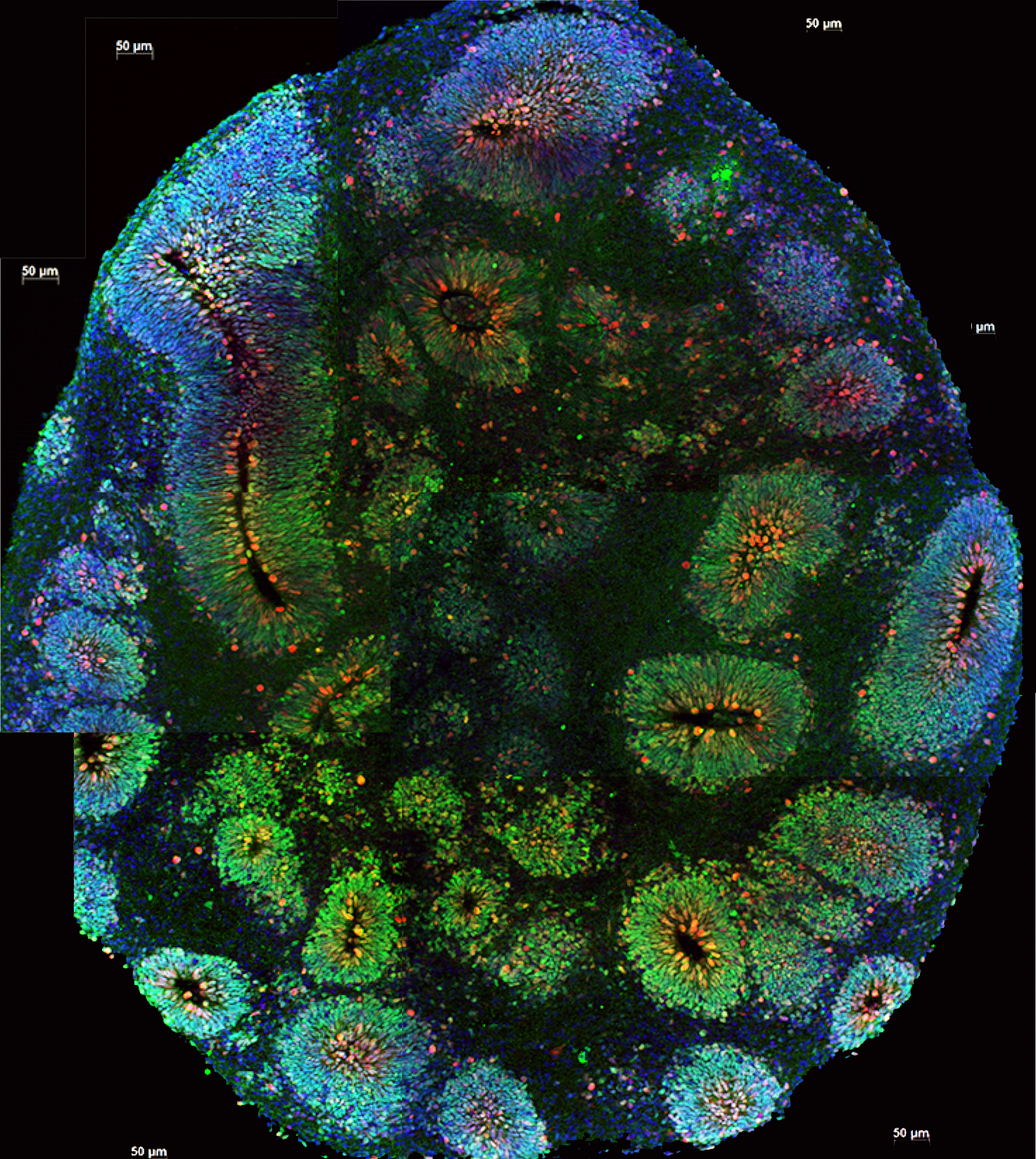
Crédito da imagem: Laboratório Vaccarino, Universidade de Yale
Para doenças cerebrais como a doença de Huntington (DH), existe uma segunda aplicação potencial poderosa para as células estaminais – o transplante. Como doença neurodegenerativa, a DH causa a perda gradual de células cerebrais. Isto acontece principalmente numa porção central do cérebro, chamada estriado, e na parte exterior enrugada do cérebro, chamada córtex.
Vários grupos de investigadores estão a explorar abordagens que lhes permitiriam aproveitar o poder das células estaminais para substituir células que são perdidas ao longo do curso da DH. Recentemente escrevemos sobre o trabalho que a Dra. Leslie Thompson está a desenvolver para transplantes de células estaminais na nossa cobertura da conferência da Hereditary Disease Foundation. Mas o que aconteceria às novas células? Adotariam características da DH?
A Dra. Elena Cattaneo e a sua equipa da Universidade de Milão, em Itália, publicaram recentemente um estudo que visa responder a algumas destas questões. O laboratório de Elena são líderes mundiais no uso de células estaminais para investigar a DH. Neste novo artigo, procuraram compreender melhor o efeito que as células com o gene da DH têm sobre as células sem o gene da DH. Isto pode ajudar a informar futuros estudos de transplante de células e ensaios que visam reduzir a mensagem causadora da doença, uma vez que é improvável que esses medicamentos atinjam todas as células do cérebro de forma igual.
Mini cérebro numa placa
Tipicamente, quando as células são usadas em experiências laboratoriais, são cultivadas de forma plana no fundo de uma placa. Mas se já viste outra pessoa, sabes que as pessoas não são 2D! Por isso, tecnologias mais sofisticadas permitem aos investigadores cultivar células em 3D.
O termo técnico para estas células 3D é “organoides”, ou seja, “mini cérebros”. Já escrevemos anteriormente sobre estes cérebros cultivados em laboratório e o que os investigadores aprenderam com eles. Embora os mini cérebros possam adotar algumas das características celulares de um cérebro, como as ligações entre diferentes células, não têm realmente a capacidade de transmitir pensamentos e sentimentos.
“Embora estes mini cérebros pareçam enganosamente pouco sofisticados por fora (como um pequeno ranho esbranquiçado e rosado, para ser honesto!), são elegantemente complexos por dentro.”
Embora estes mini cérebros pareçam enganosamente pouco sofisticados por fora (como um pequeno ranho esbranquiçado e rosado, para ser honesto!), são elegantemente complexos por dentro. As células formam redes intrincadas entre células cerebrais que podem ser vistas a comunicar umas com as outras ao microscópio. Estes mini cérebros dão aos investigadores uma forma de compreender em 3D como a DH afeta as ligações e a comunicação entre diferentes células.
Os cientistas sabem que num cérebro humano, a DH reduz a capacidade das células no córtex exterior de comunicarem com o estriado interior. Esta falha de comunicação leva a uma perda dessas ligações ao longo do tempo. Quando essas ligações ficam sem uso por longos períodos de tempo, pode criar um ambiente pouco saudável para as células cerebrais, e estas podem eventualmente morrer.
Uma influência positiva
Elena e a sua equipa veem algo semelhante nos seus mini cérebros que têm o gene da DH. A nível molecular, as células cerebrais comunicam através de um espaço muito pequeno chamado sinapse. É aqui que as extremidades das células cerebrais se encontram para enviar bolhas de informação de um lado para o outro. Na DH, o número de bolhas é reduzido ao longo do tempo. Neste novo artigo, a equipa vê o mesmo nos mini cérebros com DH – há menos comunicação na sinapse do que nos mini cérebros sem o gene da DH.
Uma experiência fundamental no novo artigo do laboratório de Elena questionou o que acontece às células em mini cérebros quando células sem o gene da DH são combinadas com células que têm o gene da DH.
A equipa realizou uma análise muito detalhada das mensagens genéticas contidas nos mini cérebros com população mista, verificando que se assemelham mais aos mini cérebros sem o gene da DH do que aos que têm o gene da DH. Isto sugere que as células sem o gene da DH têm uma influência positiva sobre as que têm o gene da DH. Bons amigos para ter por perto!
Também observaram as sinapses nestes mini cérebros com população mista. Descobriram que a comunicação enviada pela sinapse estava muito melhorada! Assemelhava-se mais aos mini cérebros sem o gene da DH. Isto sugere que as células sem DH podem estar a ajudar as células com DH a comunicar melhor.
A equipa também identificou algumas características que não foram totalmente resgatadas pela presença das células sem o gene da DH. Nos mini cérebros com população mista ainda havia algumas alterações ao nível da mensagem genética. Além disso, o número de células que morreram nos mini cérebros com população mista não foi totalmente resgatado. Isto sugere que, embora as células sem DH ajudem os mini cérebros com população mista, não conseguem superar todas as características causadas pelo gene da DH.
Informando ensaios em curso e futuros
No geral, este tipo de investigação pode ajudar a determinar o potencial terapêutico do uso de células estaminais para retardar a progressão e tratar a DH. Também é informativo para os ensaios em curso que reduzem os níveis da mensagem genética causadora da doença.
Embora o objetivo para alguns desses ensaios seja reduzir a mensagem em cerca de 50%, isso não ocorrerá em todas as células do cérebro. Por causa disso, essas células com mensagem genética da DH reduzida existirão numa população mista com células que têm mais da mensagem genética da DH. Dados de estudos como os destacados aqui ajudam os investigadores a compreender exatamente o que pode acontecer ao nível molecular quando existem tais populações mistas de células com e sem o gene da DH.
Um ponto importante que a equipa de investigação conseguiu descobrir neste artigo é que as células sem DH têm uma influência positiva nas células com o gene da DH. Mas o contrário não é verdade. As células que têm o gene da DH não parecem alterar programas nas células sem DH. Isto é importante para futuros estudos de transplante porque sugere que as células sem DH que são adicionadas podem ter um efeito positivo, mas as células já presentes no cérebro com DH possivelmente não terão um efeito negativo nas novas células. Uma vitória dupla!
“Isto sugere que as células sem o gene da DH têm uma influência positiva sobre as que têm o gene da DH. Bons amigos para ter por perto!”
Fazendo avançar os tratamentos
Embora as células estaminais e os mini cérebros sejam super interessantes, existem algumas limitações no seu uso. Em primeiro lugar, não imitam verdadeiramente o que está a acontecer dentro de um cérebro humano numa pessoa viva. Nada numa placa de laboratório consegue. É por isso que é importante estudar potenciais tratamentos num cérebro em funcionamento, como num rato, e eventualmente realizar ensaios clínicos em pessoas.
Além disso, os mini cérebros que continham células com e sem o gene da DH foram misturados antes de serem feitos. Ou seja, a população mista estava lá desde o “nascimento”. No caso de uma pessoa com DH, as células ou o tratamento seriam adicionados depois de a pessoa ter um cérebro totalmente formado.
Apesar das ressalvas, este trabalho representa uma abordagem interessante para melhor compreender como as células sem o gene da DH podem atuar se fossem adicionadas a um cérebro com DH. Também esclarece o que pode acontecer num cérebro quando algumas células têm o gene da DH enquanto outras têm menos dessa mensagem.
O cérebro humano, tanto dentro de uma placa de laboratório como fora, é incrivelmente complexo, por isso saber o máximo possível sobre como a DH afeta as características celulares e moleculares ajudará a fazer avançar os tratamentos.
Aprende mais
Para mais informações sobre a nossa política de divulgação, consulte as nossas FAQ…


