
Conferência sobre Terapêuticas para a Doença de Huntington 2023 – Dia 3
Veja as atualizações de investigação do Dia 3 da Conferência sobre Terapêuticas para a Doença de Huntington 2023 #HDTC2023.
Bem-vindos ao terceiro e último dia de ciência DH, ao vivo de Dubrovnik, Croácia!
As nossas atualizações do Twitter estão compiladas abaixo. Continue a seguir as atualizações em direto do último dia da conferência com a hashtag #HDTC2023. Veja a nossa cobertura do dia 1 aqui: https://pt.hdbuzz.net/343 e do dia 2 aqui: https://pt.hdbuzz.net/344.
Biomarcadores
A sessão desta manhã irá focar-se em biomarcadores, coisas que podemos medir para obter uma imagem da saúde de uma pessoa ou da sua resposta a um medicamento. Diferentes tipos de medições de biomarcadores podem focar-se na previsão do início, no acompanhamento da DH de uma pessoa ou na verificação da segurança de um medicamento. Como ouvimos ontem à noite, os níveis de NfL podem ajudar-nos a obter uma imagem mais precisa da saúde cerebral, mas existem outras proteínas também a serem estudadas para este propósito.
HD Clarity
O primeiro a falar é o Dr. Niels Henning Skotte, da Universidade de Copenhaga, que nos irá falar sobre o seu trabalho no estudo de biomarcadores a partir de amostras de pacientes com DH. Ele utiliza amostras de um grande estudo de recolha de fluido espinal chamado HDClarity https://hdclarity.net/. Niels está a falar primeiro sobre a importância do “controlo de qualidade” nas amostras de fluido espinal – testes que realizam para garantir que estas estão livres de contaminação e devidamente armazenadas. Ele também apresentou algumas estatísticas para mostrar quantas são necessárias para responder a diferentes tipos de questões sobre a DH. Muitas das proteínas que são potenciais biomarcadores estão presentes apenas em quantidades muito pequenas nas amostras dos pacientes.
Existem gráficos especiais chamados “gráficos de vulcão” que permitem aos investigadores ver quais as proteínas encontradas no fluido espinal que diferem mais entre pessoas com e sem o gene da DH. Alguns dos potenciais biomarcadores mostram até diferenças entre não portadores do gene e portadores pré-sintomáticos do gene, o que poderia ser útil na procura por tratamentos que possam ser administrados antes do início dos sintomas. Quando os níveis de certas proteínas diferem entre pessoas com e sem DH tanto no sangue como no fluido espinal, os investigadores analisam-nas mais detalhadamente para compreender como e possivelmente porquê os seus níveis se alteram em diferentes estadios da DH. Quando uma alteração proteica é consistente em muitas pessoas, então pode ser considerada como um biomarcador útil da DH. É considerado o papel de diferentes proteínas no corpo e como elas interagem entre si, o que pode fornecer pistas sobre os processos biológicos afetados na DH.
Nesta era da inteligência artificial ou IA, os cientistas podem alimentar sistemas computacionais com grandes conjuntos de dados e pedir-lhes para considerar conjuntos complexos de factores para determinar quais as proteínas que seriam os melhores biomarcadores. Niels está a utilizar abordagens de machine learning para fazer precisamente isso. No futuro, a medição das alterações em grupos de muitas proteínas antes do desenvolvimento de sintomas poderá ser utilizada para acompanhar melhor em que fase exata de progressão da doença uma pessoa se encontra ou para decidir quando devem começar um tratamento para a DH.
Moléculas de gordura como biomarcador para a DH
O próximo orador é o Dr. William Griffiths da Universidade de Swansea, que nos irá falar sobre como o colesterol e outras moléculas de gordura poderiam ser usados como possíveis biomarcadores para a DH. William lembra-nos que cerca de 25% do colesterol do corpo está no cérebro, e grande parte dele é produzido no local. Alguns tipos conseguem sair do cérebro, portanto, poderíamos medir os seus níveis para compreender a saúde cerebral. Perturbações do processo de produção de colesterol e alterações nos níveis de colesterol têm sido observadas na DH, e existem esforços de desenvolvimento de medicamentos focados na correção dessas alterações.
O trabalho de William foca-se em medir as diferenças nos níveis de colesterol entre pessoas com DH e pessoas sem DH, para ver se estas moléculas podem ser usadas como biomarcadores. Medir e analisar os níveis de colesterol requer técnicas avançadas de bioquímica. As moléculas específicas que eles procuram são difíceis de detetar mesmo com equipamento de ponta disponível, por isso tiveram que ajustar o sistema usando uma técnica genial chamada “química de click”. Isto aumenta o sinal do colesterol do tamanho de uma erva para o tamanho de uma árvore, como William explica. O grupo de William descobriu que uma forma de colesterol, que é gerada apenas nos neurónios, está diminuída em amostras de sangue de pacientes com DH, tornando-a um potencial biomarcador.
Instabilidade somática como marcador de DH
Agora temos o Dr. Darren Monckton, da Universidade de Glasgow, que nos irá falar sobre a investigação do seu grupo acerca da possibilidade de certos aspectos da instabilidade somática serem um biomarcador da DH.
Os cientistas conseguem medir os níveis de instabilidade somática da repetição CAG do gene da DH em vários tipos de amostras de pacientes. Darren utiliza técnicas chiques de sequenciação para fazer isso o mais precisamente possível no ADN do sangue doado por pessoas com DH. O grupo Monckton mapeou como a expansão das repetições CAG ao longo do tempo (instabilidade somática) muda em diferentes taxas em amostras de sangue, dependendo da idade da pessoa e do seu número original de repetições CAG.
Eles também analisaram amostras de sangue do mesmo indivíduo recolhidas com um intervalo de 7 anos. Isto fornece pistas sobre como a instabilidade somática aumenta em cada pessoa ao longo do tempo. Mesmo ao longo deste período de tempo enorme, as alterações geralmente são muito subtis e ocorrem lentamente. Ser capaz de medir essas pequenas mudanças é muito importante, pois potenciais medicamentos para alterar a taxa de instabilidade somática também provavelmente terão efeitos muito subtis.
Estas técnicas provavelmente serão muito úteis em alguns dos ensaios clínicos em desenvolvimento. A DH não é a única doença que apresenta instabilidade somática, e as técnicas em desenvolvimento pelo laboratório Monckton para medir pequenas alterações no ADN ao longo do tempo serão úteis para aplicar ao estudo de outras doenças genéticas e respetivos tratamentos fora do campo da DH.
Acompanhar o Huntington com traçadores PET
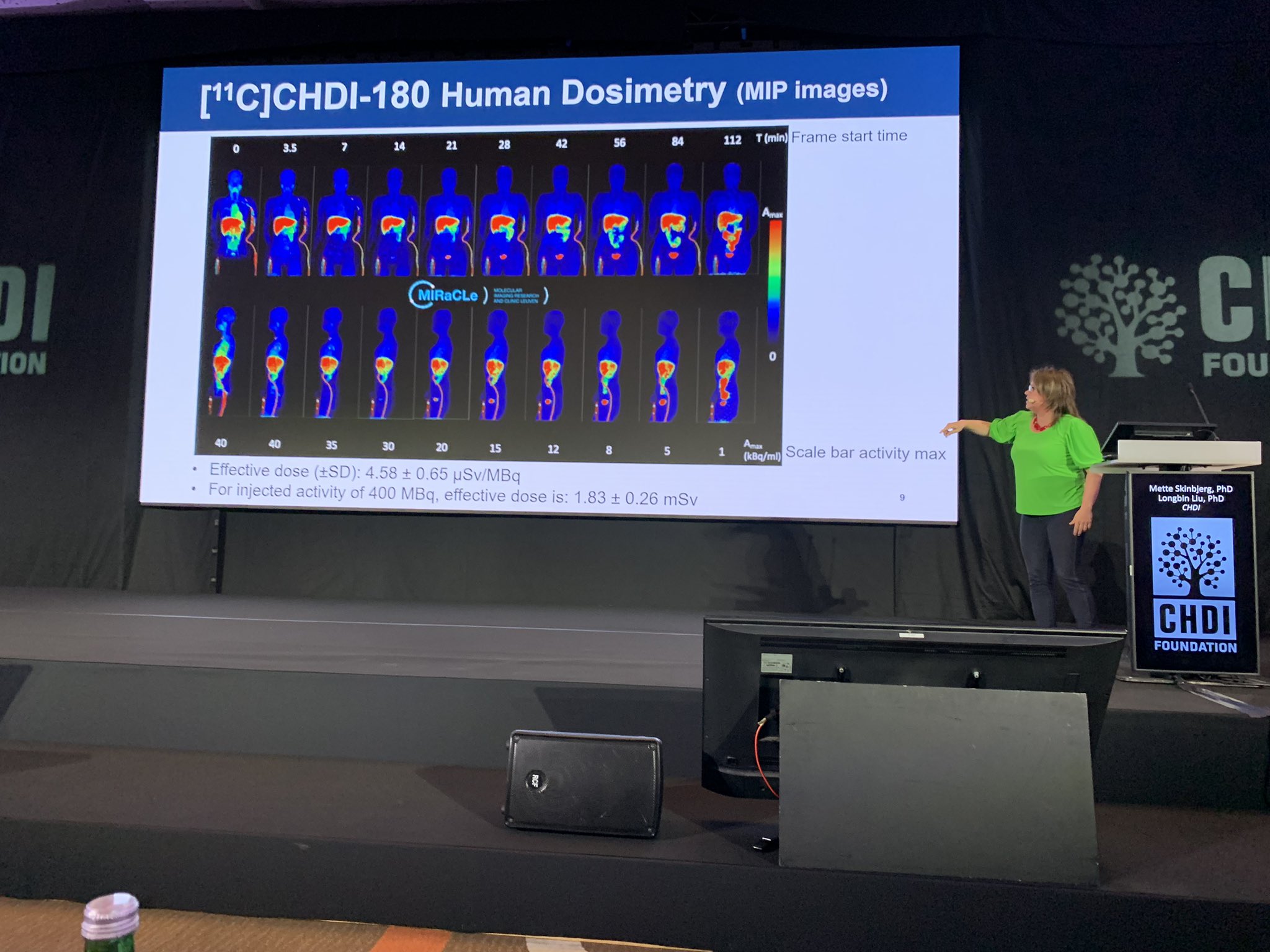
Estamos de volta da pausa para o café e agora iremos ouvir a Dra. Mette Skinbjerg falar sobre um traçador PET de huntingtina que permite rastrear os aglomerados tóxicos de proteína no cérebro que se acumulam ao longo do tempo. Já falámos sobre isso anteriormente aqui – artigo em inglês. Sem um traçador, a única forma de vermos como a proteína huntingtina se acumula no cérebro humano é ao examinarmos amostras após o falecimento de alguém. Os traçadores são uma forma segura de fazer observações em pessoas vivas e podem ser uma excelente forma de vermos como os medicamentos podem estar a funcionar.
A CHDI tem trabalhado com parceiros académicos para desenvolver um traçador para a DH, que eles caracterizaram extensivamente em diversos modelos animais de DH, incluindo ratos e macacos, o que permite rastrear a acumulação de aglomerados de proteína ao longo do tempo. Agora estão a avançar além dos modelos animais para testar o seu traçador em pessoas. Os traçadores são marcados com radioatividade, para que os cientistas possam medir onde eles se ligam ao alvo – neste caso, os aglomerados. É importante que os traçadores sejam eliminados do corpo após a administração, para que a exposição à radioatividade esteja dentro da janela segura.
Embora o traçador pareça ser seguro para uso em pessoas, infelizmente, o sinal no cérebro não acompanhou o que os cientistas esperavam. Isto é dececionante, mas este programa ensinou-nos muito sobre como desenvolver um traçador para a DH, o que pode ser utilizado para criar traçadores melhores no futuro. Agora, a equipa está a trabalhar numa nova geração de traçadores, com a esperança de que funcionem muito melhor. As coisas estão a progredir no laboratório, com muitos testes em animais com DH, por isso esperamos que esta próxima ronda seja mais bem-sucedida.
Biomarcadores e machine learning
O próximo orador é o Dr. Peter Wijeratne, da Universidade de Sussex. O grupo do Peter tem como objetivo utilizar biomarcadores e machine learning para caracterizar e prever a progressão da DH em indivíduos. fixe!
À medida que os investigadores continuam a identificar diversos biomarcadores a partir de fluidos biológicos, imagem, etc., muitos biomarcadores de uma pessoa podem ser combinados para obter melhores previsões. No entanto, combinar e compreender todos estes dados em conjunto é difícil para as pessoas fazerem, é aqui que a IA nos pode ajudar!
Peter utilizou um exemplo divertido com o ChatGPT para explicar machine learning – um algoritmo que pode adaptar-se e fazer inferências a partir de padrões nos dados. Ele mostrou quão rapidamente estes sistemas podem aprender novas informações e tomar decisões fundamentadas – muito fixe! Para “treinar” o sistema de IA, é necessário ter muitos e muitos dados de treino de alta qualidade, para os quais os cientistas já conhecem as respostas. O sistema de IA pode então aprender a identificar padrões nesses dados, permitindo-lhe detetar padrões semelhantes e relacionados nos dados de teste, onde as respostas ainda não são conhecidas.
O grupo de Peter está a analisar dados de imagens cerebrais de três estudos diferentes que examinaram como diferentes estruturas cerebrais se alteram ao longo do tempo na DH. Ao treinar a IA com estes conjuntos de dados complexos e ricos, eles esperam conseguir fazer previsões sólidas sobre a doença. Pelos vistos é possível obter boas previsões para o início da doença, e os resultados foram concordantes com o sistema de estadiamento HD-ISS. Esperam que isso se revele útil para fazer previsões ao nível individual no futuro.
Níveis de HTT e tominersen
Na próxima palestra, o Dr. Blair Leavitt, um clínico/investigador da Universidade da Colúmbia Britânica, irá falar sobre o seu estudo de amostras do ensaio GEN-EXTEND com o tominersen. Ele está a investigar mais a fundo como os níveis de huntingtina mudam com o tratamento com tominersen.

Blair começa por agradecer aos membros das famílias afetadas pela DH que generosamente e altruísticamente partilham amostras biológicas com os cientistas para criar um recurso de biobanco. Isto é de valor inestimável para os cientistas compreenderem a DH e como os medicamentos podem alterar o curso desta doença. Blair está a focar-se num indivíduo em particular, que quis muito doar o seu cérebro após o seu falecimento. Um conjunto de dados rico e muitas amostras estão disponíveis a partir dos ensaios com tominersen em que ele participou, juntamente com o tecido cerebral, o que oferece uma oportunidade rara para observar os efeitos do medicamento.
Ao analisar o cérebro, os cientistas da equipa de Blair conseguiram medir os níveis do fármaco em diferentes regiões e compará-los com os níveis de exposição previstos por experiências anteriores em macacos. Em geral, os resultados mostraram que as previsões eram bastante precisas. Em seguida, analisaram os níveis de huntingtina em diferentes regiões do cérebro e como se comparam com cérebros de controlo. Como esperado para um tratamento que reduz os níveis de huntingtina, os níveis neste indivíduo eram muito mais baixos do que nos controlos. Infelizmente, os níveis de huntingtina no líquido espinal eram demasiado baixos para serem quantificados neste indivíduo. Isto significa que não sabemos quão bem os níveis de huntingtina no cérebro e no líquido espinal se correlacionam, pelo menos para este participante no ensaio.
É difícil exagerar a importância deste tecido para os cientistas, pois permite examinar em profundidade como um tratamento afetou o cérebro. Colaboradores na audiência farão perguntas adicionais utilizando este tecido generosamente doado por este participante do ensaio.
Ensaios clínicos
Após uma pausa para almoço, estamos de volta para a última sessão científica da conferência #HDTC2023. A sessão desta tarde será dedicada aos ensaios clínicos e iremos ouvir sobre desenho de estudo e avanços na investigação em seres humanos.
Classificar os estadios da DH
O Dr. Jeff Long, da Universidade de Iowa, está a falar sobre o HD-ISS, um sistema de classificação para a DH. É uma ferramenta de investigação clínica que permite aos investigadores melhor classificar as pessoas nos estadios iniciais da DH, com vista a um desenho de ensaios e recrutamento mais eficientes.
Agora que esta nova ferramenta está a ser mais amplamente utilizada, a equipa do Jeff está a desenvolver uma base de dados com informações de grandes estudos observacionais, como o IMAGE-HD, PREDICT-HD, TRACK-HD e ENROLL-HD, para compreender melhor o curso da progressão através dos estadios do HD-ISS. Após a construção destas ferramentas, a equipa do Jeff está a trabalhar para perceber como seriam úteis num ensaio clínico – quantos pacientes com DH num determinado estadio da doença seriam necessários para obter resultados sólidos capazes de nos convencer se um medicamento funcionou ou não.
Uma vez que o HD-ISS incorpora dados de imagens cerebrais, biomarcadores e genética, muitas variáveis podem ser consideradas para definir quais são as medições clínicas mais adequadas para mostrar se um novo fármaco pode estar a funcionar. Ao utilizar bases de dados de estudos observacionais, investigadores como o Jeff podem aplicar técnicas estatísticas para prever melhor quantos participantes e que tipo de avaliações poderão ser necessários para demonstrar o benefício de um fármaco. Esta é uma matemática complexa e importante que ilustra a importância da participação em investigação observacional.
A prova dos factos
A próxima apresentação é muito aguardada, pois irá partilhar os resultados muito iniciais do Ensaio PROOF-HD com a Pridopidina. Na terça-feira, ficámos a saber pelos meios de comunicação social que o ensaio não atingiu os seus objetivos primários, mas agora estamos a ver os dados.
O Dr. Michael Hayden, CEO da Prilenia, está a fazer esta apresentação. Ele começa por explicar o mecanismo pelo qual se acredita que o fármaco afeta as células nervosas, em particular a sua ação num tipo de recetor que facilita a comunicação entre os neurónios, conhecido como sigma 1.
O ensaio PROOF-HD foi concebido para utilizar determinadas avaliações clínicas, uma combinação de testes de movimento, comportamento e cognição, para ver se a pridopidina ajudava a abrandar a progressão dos sintomas da DH ao longo de cerca de um ano e meio. Os ensaios são concebidos com “objetivos primários”, “secundários” e “exploratórios”. Demonstrar que um fármaco afeta os objetivos primários é geralmente como se tomam decisões para continuar a desenvolver o fármaco e, eventualmente, obter a sua aprovação. Este ensaio recrutou rapidamente, e a maioria dos participantes permaneceu nele durante todo o período, o que é um testemunho da mobilização e do compromisso dos pacientes com DH. Quando a grande maioria das pessoas continua num ensaio longo, isso também pode ser indicativo da segurança e tolerabilidade do fármaco.
O principal resultado global é que os objetivos principais do ensaio não foram alcançados. Neste caso, era uma medição da capacidade das pessoas para funcionarem no dia-a-dia. Em média, as pessoas que tomaram pridopidina e as pessoas que tomaram placebo tiveram um funcionamento semelhante ao longo do ensaio. Outro objetivo importante consistia numa combinação de diferentes medidas de movimento, comportamentais e cognitivas, que também não melhoraram nas pessoas que tomaram pridopidina. A pridopidina poderá ter mostrado alguns benefícios numa medição de movimento chamada Q-motor, mas isso não foi estatisticamente significativo.
Quando um ensaio é planeado, mas antes de começar, o promotor (neste caso, a Prilenia) tem de tomar decisões sobre que tipos de estatísticas e análises serão realizados quando os resultados estiverem disponíveis. No PROOF-HD, a Prilenia decidiu separar os grupos de participantes entre aqueles que tomavam fármacos chamados neurolépticos (também conhecidos como psicotrópicos) e aqueles que não tomavam neurolépticos. Isto ocorre porque a pridopidina afeta algumas das mesmas vias biológicas que os neurolépticos. Quando a Prilenia analisou os dados apenas das pessoas que não estavam a tomar fármacos neurolépticos, o potencial benefício tornou-se mais evidente em algumas medições clínicas, especialmente no primeiro ano. No entanto, no final, isto também não foi estatisticamente significativo.
Michael está agora a apresentar os dados de um ensaio com pridopidina em pessoas com ELA, uma doença que partilha algumas características biológicas com a DH. Este ensaio também mostrou alguns benefícios potenciais em resultados secundários.
A Prilenia acredita que ainda existe alguma esperança para a pridopidina no tratamento da DH, e a empresa irá agora concentrar-se em analisar mais detalhadamente os dados. Eles precisam especialmente de compreender como diferentes tratamentos neurolépticos afectam a resposta ao fármaco.
Luz vermelha para o branaplam
A seguir, a Dra. Beth Borowsky, da Novartis, descreve os resultados do seu ensaio com um fármaco chamado branaplam em pacientes com DH. Falámos sobre este fármaco e o seu surpreendente mecanismo de ação aqui – artigo em inglês.
Embora o branaplam fosse seguro em crianças com outra doença (atrofia muscular espinal), alguns estudos em animais indicaram a possibilidade de danos nos nervos que projetam do cérebro para a pele e músculos do corpo. Com base nessa preocupação, a Novartis incluiu especialistas especializados nesse tipo de danos nervosos em pacientes com DH tratados, apenas para o caso de surgir algum sintoma durante o ensaio.
Infelizmente, ao longo de algumas semanas, algumas medições subtis de movimento e laboratoriais começaram a sugerir que os receios de facto tinham surgido. Em consulta com os seus monitores de segurança independentes, a Novartis decidiu interromper inicialmente a administração. No momento da interrupção, os pacientes tinham recebido tratamento durante 5 a 22 semanas. Após uma revisão cuidadosa, verificou-se que 78% dos pacientes tratados mostraram um ou mais sinais que poderiam indicar danos nos nervos, e também algumas alterações nas estruturas cerebrais chamadas ventrículos.
Com base numa análise muito cuidadosa do benefício e do risco para os pacientes, a Novartis tomou a decisão de interromper o ensaio em dezembro de 2022. Falámos sobre isso aqui. Atualmente, todos os participantes no ensaio continuam a ser monitorizados quanto a sintomas de danos nos nervos e para acompanhar como isso pode evoluir ao longo do tempo após terem interrompido a administração do fármaco.
Beth trouxe uma amostra de dados que a Novartis recolheu para atualizar a comunidade da DH sobre o que encontraram. Primeiro – como esperado, o branaplam reduziu os níveis de Huntingtina em cerca de 25% no líquido espinal, sugerindo que o branaplam foi capaz de diminuir os níveis de Huntingtina no cérebro.
Infelizmente, a Novartis também encontrou níveis mais elevados de uma proteína chamada neurofilamento leve, ou NfL, um marcador de células cerebrais infelizes. Já falámos sobre o NfL antes, uma vez que este aumenta no curso normal da DH, e foi um foco importante na sessão de biomarcadores deste encontro. Esperaríamos que, se um fármaco para a DH funcionasse, os níveis de NfL diminuíssem ao longo do tempo. No entanto, no estudo com o branaplam, a Novartis descobriu que os níveis de NfL no sangue e no líquido espinal aumentaram com o tratamento. Esta é uma das descobertas que ajudaram a incentivar a Novartis a pausar o estudo.
Em paralelo a estes testes laboratoriais, os médicos estavam a realizar estudos cuidadosos da função nervosa em cada participante. Cerca de 86% dos participantes apresentou algum tipo de sintoma neurológico, e as imagens cerebrais mostraram cavidades cheias de líquido maiores, conhecidas como ventrículos laterais.
No conjunto, parece que o fármaco da Novartis fez o que se esperava – reduzir os níveis de Huntingtina no cérebro. Infelizmente, isto foi acompanhado por efeitos secundários graves, pelo que não existe um caminho seguro para avançar com este fármaco. É importante salientar que a Novartis continua a monitorizar os participantes do ensaio e a analisar os dados para orientar o desenvolvimento de fármacos no futuro.
O AMT-130 avança
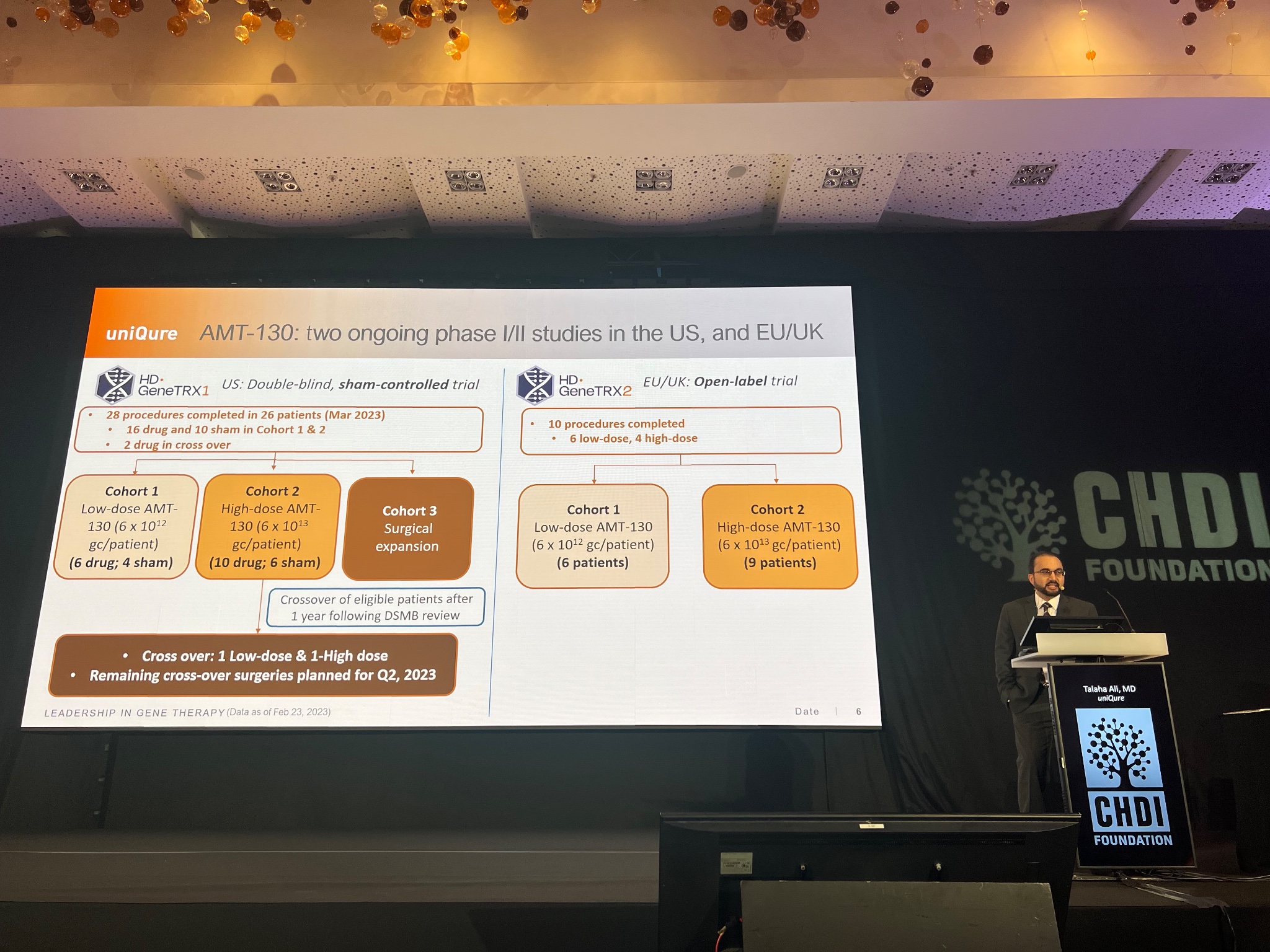
A seguir, o Dr. Talaha Ali, da uniQure, está a apresentar uma atualização sobre o estudo da sua terapia genética para a DH, chamada AMT-130. Esta terapia baseia-se na injeção de vírus inofensivos que transportam instruções para ensinar as células cerebrais a reduzir os níveis de HTT.
O incrível destas terapias genéticas virais é que teoricamente requerem apenas uma única injeção, uma vez que os vírus persistem no cérebro durante muitos anos – talvez para sempre. O lado negativo é que requer cirurgia para administrar os vírus no cérebro. Esta abordagem cirúrgica está a ser testada em dois ensaios separados – um nos Estados Unidos e outro na Europa. Devido a ser uma tecnologia tão avançada, apenas um número reduzido de pessoas está a ser incluído – cerca de 40 pacientes no total.
Os pacientes no ensaio recebem injeções muito cuidadosas e lentas do fármaco em diferentes partes das estruturas profundas do cérebro que são mais afetadas na DH. O ensaio está a testar uma dose baixa e uma dose alta de AMT-130, e a monitorizar de perto os participantes durante o primeiro ano e, em seguida, com maior frequência por até 5 anos. A uniQure irá partilhar novos dados e atualizações em breve, provavelmente até ao final de junho de 2023.
Como reportado anteriormente,ao longo do caminho, a uniQure teve algumas reações preocupantes em três pacientes. Após uma análise cuidadosa, os médicos independentes responsáveis por monitorizar estes sintomas decidiram que o risco parecia aceitável, e o ensaio clínico continuou.
O que é entusiasmante é que a uniQure tem algumas evidências de que o AMT-130 reduz os níveis de Huntingtina no líquido cefalorraquidiano (LCR) – mas até ao momento o número de pacientes tratados é demasiado pequeno para fazer estimativas precisas. Esperamos que haja mais dados empolgantes da próxima vez que ouvirmos falar da uniQure!
Estreitando os alvos para o tominersen
A próxima palestra é do Dr. Peter McColgan da Roche, que está a desenvolver um medicamento chamado tominersen para a DH. Ele falará sobre a história do programa, o que estão a aprender com os ensaios clínicos do tominersen e o que está a acontecer com o ensaio clínico GENERATION HD2 em curso.
Inicialmente, o tominersen foi desenvolvido pela Ionis, um medicamento genético administrado através da coluna vertebral, chamado um ASO. Em ensaios clínicos iniciais e de curta duração para avaliação de segurança, foi o primeiro medicamento capaz de reduzir os níveis de huntingtina em humanos. Isto foi seguido por um ensaio clínico muito grande para testar os efeitos nos sintomas da DH, conhecido como GENERATION HD1. Em março de 2021, descobrimos que o GENERATION HD1 foi interrompido devido a preocupações com a segurança – o tominersen não estava a ajudar os pacientes com DH e, na dose mais alta, poderia até estar a causar danos.
Mais tarde, a Roche aprofundou a análise dos dados e descobriu que alguns participantes no estudo GENERATION HD1 podem ter beneficiado do tominersen, especificamente aqueles que iniciaram o ensaio numa idade mais jovem e com sintomas menos graves. Por essa razão, a Roche projetou e lançou o ensaio GENERATION HD2, que é um estudo menor que testa o tominersen numa população mais jovem nos estadios iniciais da DH. Este estudo está atualmente em recrutamento e eventualmente haverá até 75 centros em 15 países.
Agora o Peter está a apresentar dados sobre a NfL, uma proteína que pode servir como um marcador de danos nas células nervosas. Novas análises dos dados do estudo GENERATION HD1 mostram que administrar o tominersen em doses mais baixas é provavelmente mais seguro, com base nos níveis mais baixos de NfL. O ensaio GENERATION HD2 está a testar dois níveis diferentes e mais baixos de tominersen, e modelos matemáticos preveem que estas doses mais baixas serão mais seguras, pois não levarão a aumentos tão grandes de NfL.
Agora, Peter está a partilhar novos dados sobre a NfL do ensaio GENERATION HD1. No final do estudo, parece realmente que os níveis de NfL estão a diminuir com o tominersen, o que é mais uma evidência de que as doses mais baixas em teste no GENERATION HD2 podem ter alguma promessa.
Aqui está toda a apresentação do Peter sobre o tominersen.
E assim terminam as apresentações de investigação na Conferência sobre Terapêuticas para a Doença de Huntington 2023. Obrigado por acompanhar e visite http://hdbuzz.net para ler resumos do Dia 1, Dia 2 e Dia 3!
Para mais informações sobre a nossa política de divulgação, consulte as nossas FAQ…


